유기 화학물 - 알케인, 입체화학
1. 작용기 및 유기 화합물 분류
1.1 작용기의 정의와 역할
작용기 (Functional Group)는 분자 내에서 특징적인 화학 반응성을 나타내는 원자 또는 원자단의 집합이다. 유기 분자의 화학적 거동은 분자의 크기나 복잡성과 관계없이 주로 그 작용기에 의해 결정된다. 작용기의 구조적 특징에 따라 유기 화합물들을 여러 계열로 분류한다.
1.2 주요 작용기 유형
유기 화합물은 구조적 특징에 따라 크게 세 가지 유형의 작용기로 분류된다.
탄소-탄소 다중 결합: 알켄 (이중 결합), 알카인 (삼중 결합), 아렌 (방향족 고리) 등이 있다.
탄소와 전기음성 원소의 단일 결합:
할로젠화 알킬 (
\text{C}-\text{X} ), 알코올 (\text{C}-\text{OH} ), 에터 (\text{C}-\text{O}-\text{C} ), 아민 (\text{C}-\text{N} ), 싸이올 (\text{C}-\text{SH} ) 등이 포함된다.이러한 결합은 극성을 띠며, 전기음성도가 높은 원소가 전자를 끌어당겨 탄소는 부분 양전하 (
\delta+ )를, 전기음성 원소는 부분 음전하 (\delta- )를 갖게 된다.
카보닐기 (
\text{C}=\text{O} ):
카보닐기 (Carbonyl Group)는 탄소와 산소의 이중 결합으로 이루어진 작용기이다.
\text{C}=\text{O} 결합은 극성 이중 결합이며, 카보닐 탄소는\delta+ 를, 산소는\delta- 를 가진다.카보닐 탄소에 결합된 원자에 따라 알데하이드, 케톤, 카복실산, 에스터, 아마이드 등 다양한 유도체로 존재한다.
1.3 분자 간 힘과 물리적 성질
유기 화합물의 끓는점, 녹는점, 용해도와 같은 물리적 성질은 분자 간의 인력인 분자 간 힘 (Intermolecular Forces)에 의해 결정된다.
분산력 (Dispersion Force): 모든 유기 분자 사이에 존재하며, 분자량이 클수록, 표면적이 넓을수록 강하게 작용한다.
쌍극자-쌍극자 상호작용 (Dipole-Dipole Interaction):
\text{C}-\text{X} ,\text{C}=\text{O} 와 같이 극성 결합을 가진 분자 사이에 작용하며, 분산력보다 더 강한 인력을 제공한다.수소 결합 (Hydrogen Bonding):
\text{F} ,\text{O} ,\text{N} 원자에 직접 결합된 수소 원자 (\text{H} )와 이웃 분자의\text{F} ,\text{O} ,\text{N} 원자의 비공유 전자쌍 사이에 작용하는 매우 강한 쌍극자-쌍극자 상호작용이다. 알코올, 카복실산, 아민 등은 수소 결합을 형성하여 끓는점이 현저히 높아진다.
2. 알케인의 특성과 구조 이성질체
2.1 알케인의 정의와 반응성
알케인 (Alkane)은
2.2 구조 이성질체와 물리적 성질
구조 이성질체 (Constitutional Isomer): 동일한 화학식을 가지지만, 원자들의 결합 순서가 서로 다른 화합물이다. 알케인은 직선 사슬 형태와 가지 달린 사슬 형태로 존재한다.
끓는점과 녹는점: 분자량이 증가함에 따라 분산력이 커지므로 끓는점과 녹는점이 규칙적으로 증가한다.
곁가지 효과: 곁가지가 많아질수록 분자가 구형에 가까워져 표면적이 작아진다. 이에 따라 분산력이 감소하여 끓는점이 낮아진다.
2.3 알킬기와 탄소의 차수
알킬기 (Alkyl Group): 모체 알케인에서 수소 원자 하나가 제거되어 남은 부분 구조이며, 이름은 모체 알케인의 접미사 ‘-ane’를 ‘-yl’로 바꾸어 명명한다.
탄소의 차수: 탄소 원자에 결합된 다른 탄소 원자의 수에 따라 일차 (
\text{1}^\circ ), 이차 (\text{2}^\circ ), 삼차 (\text{3}^\circ ), 사차 (\text{4}^\circ )로 구분한다. 수소 원자 역시 결합된 탄소의 차수에 따라 일차, 이차, 삼차 수소로 구분한다.
3. 알케인의 명명법 (IUPAC)
IUPAC 명명법은 유기 화합물의 이름을 접두사 (치환기), 주 작용기 자리 (위치), 모체 (탄소 수), 접미사 (주 작용기)의 네 부분으로 체계화하는 규칙이다.
3.1 명명 규칙 (가지 달린 알케인)
모체 탄화수소 찾기: 분자 내 가장 긴 연속된 탄소 사슬을 찾는다. 길이가 같은 사슬이 여러 개일 경우 가장 많은 수의 곁가지를 가진 사슬을 모체로 선택한다.
번호 붙이기: 첫 번째 곁가지 점에 가장 가까운 끝에서부터 모체 사슬의 탄소에 번호를 붙인다.
치환기 확인 및 번호 부여: 모체 사슬에 붙은 각 치환기에 위치 번호 (Locant)를 부여한다. 같은 탄소에 두 개의 치환기가 있으면 같은 번호를 두 번 겹쳐 부여한다.
이름 작성:
정렬: 둘 이상의 치환기는 알파벳순으로 나열한다.
접두사:
\text{Di-} ,\text{tri-} ,\text{tetra-} 등의 곱수 접두사는 알파벳순 나열에 사용하지 않는다.구분: 번호와 번호는 쉼표 (,)로, 번호와 접두사는 하이픈 (-)으로 분리한다.
4. 입체화학과 형태 이성질체
4.1 입체화학 및 형태
입체화학 (Stereochemistry)은 분자들의 삼차원적인 모양과 공간 배열을 연구하는 화학 분야이다.
형태 (Conformation): 단일 결합의 회전으로 인해 원자들의 공간 배열이 달라진 배열이다.
형태 이성질체 (Conformer): 서로 다른 형태를 가진 분자들을 뜻하며, 상호 변환이 매우 빨라 보통 분리되지 않는다.
4.2 형태 표현법과 안정성
단일 결합의 회전 에너지 장벽은 작지만, 모든 형태가 동일하게 안정하지는 않다.
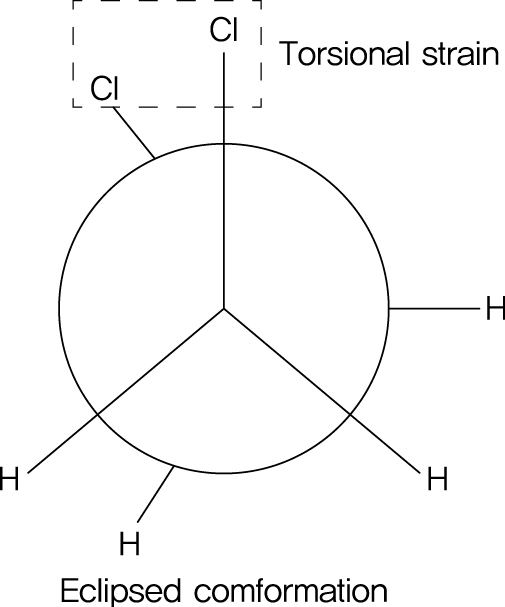
Newman 투영도 (Newman Projection):
\text{C}-\text{C} 결합 축을 정면으로 바라보며 앞뒤 탄소의 결합 배열을 원과 선으로 나타내는 표현법이다.
엇갈린 형태 (Staggered Conformation): 에너지 장벽이 가장 낮은 가장 안정한 형태이다. 결합들이 서로 최대한 멀리 떨어져 있다 (이면각
\text{ 60}^\circ ).가려진 형태 (Eclipsed Conformation): 에너지 장벽이 가장 높은 가장 불안정한 형태이다. 결합들이 서로 가장 가까이 놓여 있다 (이면각
\text{ 0}^\circ ).
4.3 형태의 불안정성 요인 (무리, Strain)
형태의 불안정성은 다음 두 가지 요인에서 발생한다.
비틀림 무리 (Torsional Strain):
\text{C}-\text{H} 결합들이 서로 가려져서 발생하는 여분의 에너지이다. 에테인의 가려진 형태에서 약\text{12 kJ/mol} 의 에너지가 발생한다.입체 무리 (Steric Strain): 허용된 원자 반지름보다 큰 원자단들이 서로 가까이 놓일 때 발생하는 반발성 상호작용이다.
부테인 형태의 상대적 안정성
부테인의
\text{C}2-\text{C}3 결합 회전 시 큰 치환기 (\text{CH}_{3} 기) 간의 상호작용이 안정성을 결정한다.
안티 형태 (Anti Conformation): 두 개의 큰 치환기 (
\text{CH}_{3} 기)가 서로\text{180}^\circ 떨어져 있는 가장 낮은 에너지의 엇갈린 배열이다.고쉬 형태 (Gauche Conformation): 두 개의 큰 치환기가 서로
\text{60}^\circ 떨어져 있는 엇갈린 배열이다. 입체 무리가 발생하여 안티 형태보다 약\text{3.8 kJ/mol} 높은 에너지를 가진다.결론: 알케인에서 가장 바람직한 형태는 큰 치환기들이 서로 안티 (anti)로 정렬된 엇갈린 배열이다.
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기