전기화학
1. 전기화학의 기초: 산화-환원 반응 (Fundamentals of Electrochemistry: Redox Reactions)
1.1. 전기화학의 정의
전기화학 (Electrochemistry)은 화학 에너지와 전기 에너지의 상호 전환을 다루는 화학 분야이다. 자발적인 화학 반응을 전기 에너지로 변환하거나, 전기 에너지를 사용하여 비자발적인 화학 반응을 유도한다.
1.2. 산화-환원 반응 (Redox Reactions)
산화 (Oxidation): 전자를 잃는 과정이다. 산화수가 증가된다.
환원 (Reduction): 전자를 얻는 과정이다. 산화수가 감소된다.
산화제 (Oxidizing Agent): 상대 물질을 산화시키고 자신은 환원되는 물질이다.
환원제 (Reducing Agent): 상대 물질을 환원시키고 자신은 산화되는 물질이다.
반쪽 반응 (Half-Reaction): 산화 반응과 환원 반응을 별도의 식으로 분리하여 전자 이동을 명확히 나타낸 반응이다.
2. 갈바니 전지와 전지 전위 (Galvanic Cells and Cell Potential)
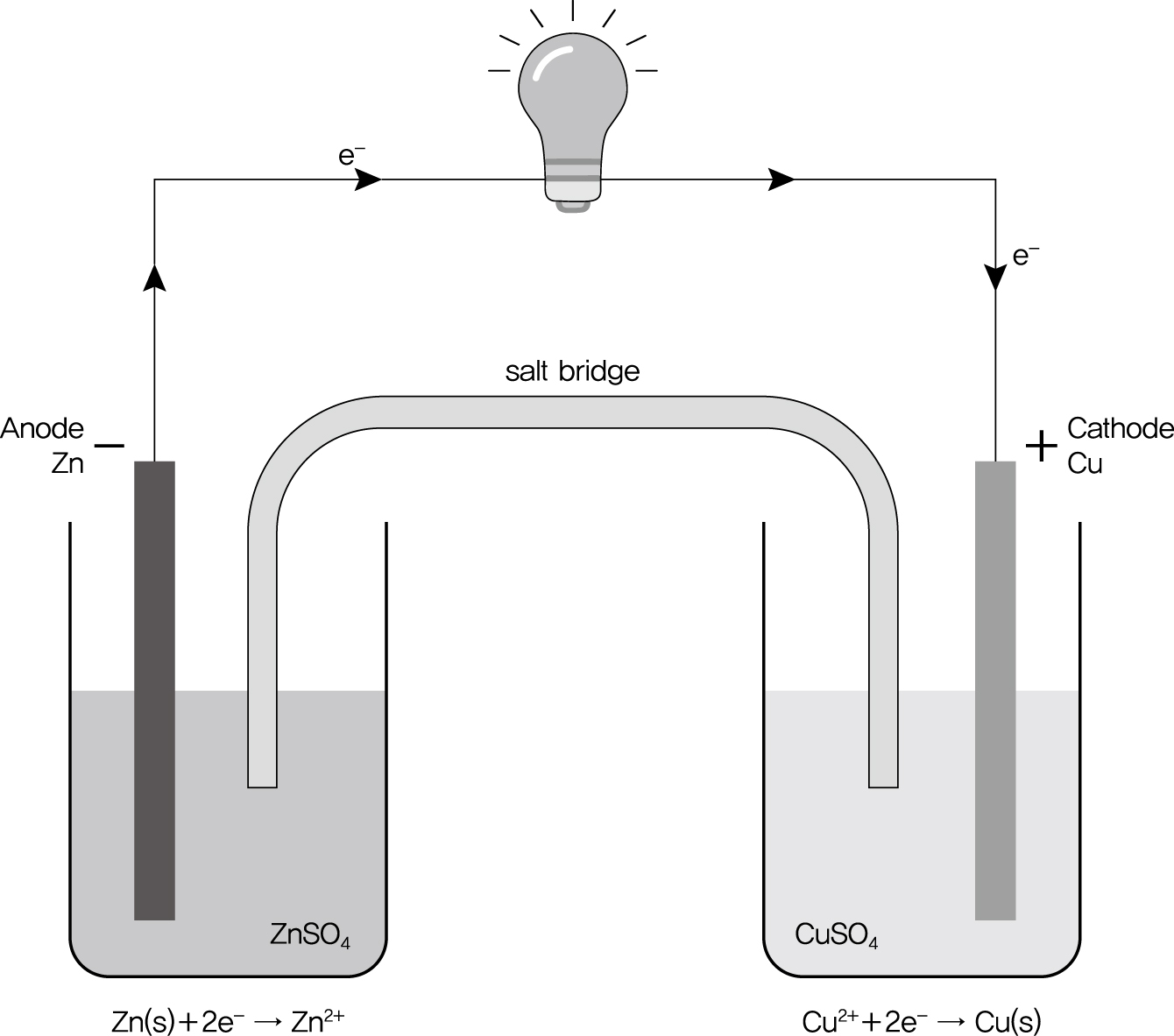
2.1. 갈바니 전지 (Galvanic Cell / Voltaic Cell)
정의: 자발적인 산화-환원 반응을 이용하여 화학 에너지를 전기 에너지로 직접 변환하는 장치이다.
전극의 구분:
음극 (Anode): 산화 반응이 일어나는 전극이며, 전자를 방출한다.
양극 (Cathode): 환원 반응이 일어나는 전극이며, 전자를 받아들인다.
염다리 (Salt Bridge): 두 반쪽 전지(
2.2. 전지 전위 (
전기 기전력 (
표준 수소 전극 (
표준 환원 전위 (
표준 전지 전위 (
3. 전기화학 반응의 열역학 및 농도 영향 (Thermodynamics and Concentration Effects)
3.1. 깁스 에너지 및 평형 상수와의 관계
표준 깁스 에너지 (
평형 상수 (
3.2. 네른스트 식과 농도 효과 (Nernst Equation)
네른스트 식: 표준 조건(
전지 반응이 평형(Equilibrium)에 도달하면
4. 응용 분야 (Applications of Electrochemistry)
4.1. 전지 및 연료 전지 (Batteries and Fuel Cells)
전지 (Batteries): 갈바니 전지 원리를 활용하여 화학 에너지를 전기 에너지로 저장하고 공급하는 장치이다.
연료 전지 (Fuel Cells): 연속적인 반응물(예: 수소)의 공급을 통해 전기 에너지를 지속적으로 생성하는 전지이다.
4.2. 부식 (Corrosion)
정의: 금속이 자발적인 산화-환원 반응을 통해 산화되어 성질이 저하되는 현상이다. 전기화학적 과정에 해당된다.
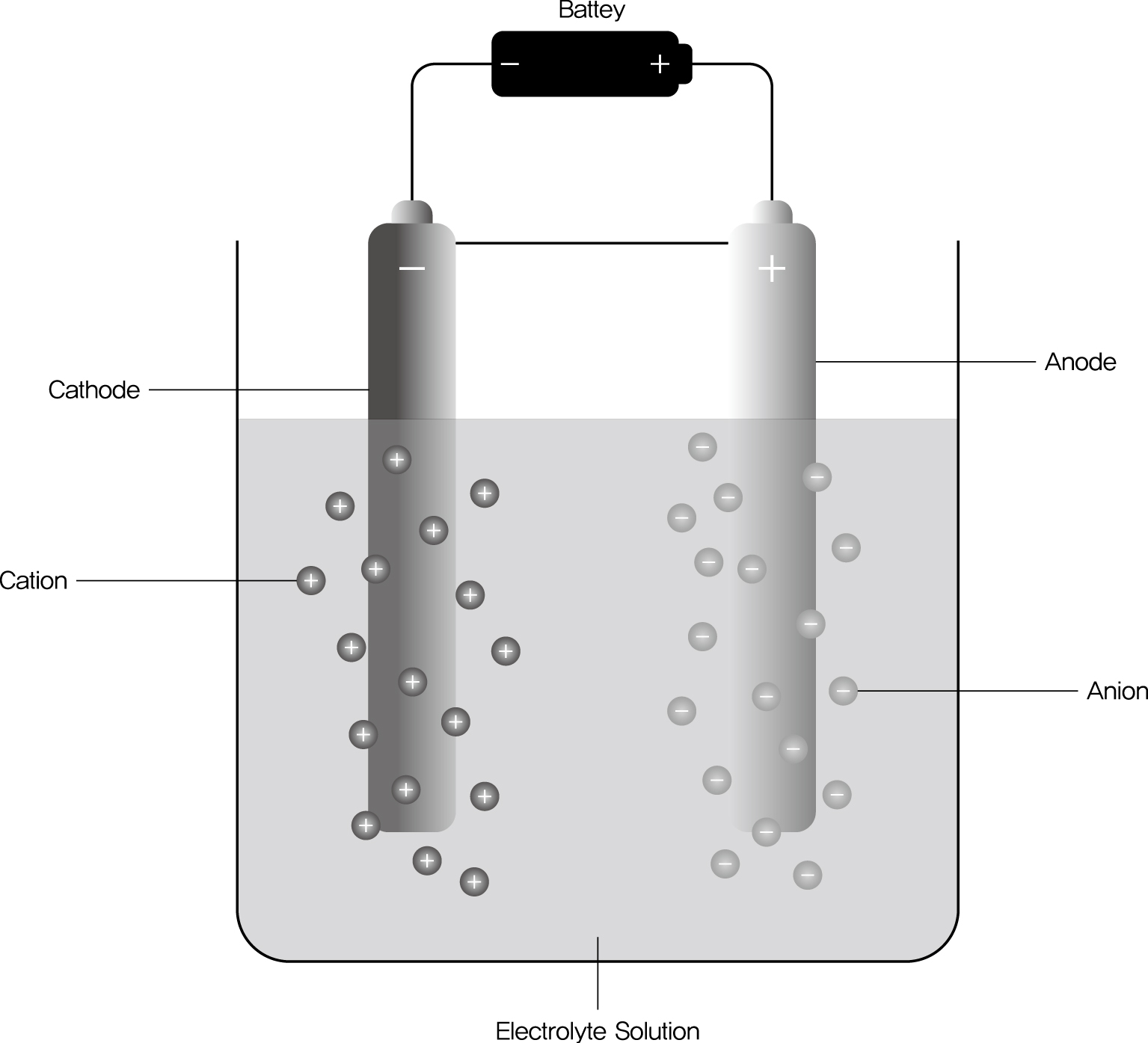
4.3. 전기분해 (Electrolysis)
정의: 전기 에너지를 사용하여 비자발적인 산화-환원 반응(
원리: 외부 전압을 인가하여 음극에서는 환원(Cathode)을, 양극에서는 산화(Anode)를 유도한다. 전기 도금(Electroplating)이나 금속의 순수화 등에 활용된다.
패러데이 법칙: 전기분해를 통해 소모되거나 생성되는 물질의 양(몰수)은 흐르는 전기량(전류 × 시간)에 정비례한다.
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기