분자간 힘과 액체 및 고체
1. 분자간 힘의 본질 (Nature of Intermolecular Forces)
1.1. 분자간 힘과 분자 내 힘 (Intermolecular vs. Intramolecular Forces)
분자간 힘 (Intermolecular Forces): 분자 사이에 작용하는 인력이며, 물질의 물리적 상태(기체, 액체, 고체)와 물리적 특성(끓는점, 녹는점)을 결정하는 데 중요한 역할을 한다.
분자 내 힘 (Intramolecular Forces): 분자 안의 원자들을 서로 묶어주는 힘으로, 주로 공유 결합이나 이온 결합을 의미한다.
상대적인 세기: 분자 내 힘(화학 결합)은 일반적으로 분자간 힘보다 훨씬 강하다. 분자 내 결합 에너지는 수백
\text{kJ/mol} 인 반면, 분자간 힘의 세기는 보통 수\text{kJ/mol} 에 불과하다.
1.2. 분자간 힘의 종류 (Types of Intermolecular Forces)
분자간 힘은 세 가지 주요 범주로 분류된다:
1.2.1. 쌍극자-쌍극자 힘 (Dipole-Dipole Forces)
정의: 극성 분자(쌍극자 모멘트가 0이 아닌 분자) 사이에 존재하는 분자간 인력이다.
원리: 극성 분자들은 영구적인 부분적인 전하를 가지며, 한 분자의 양전하 부분은 이웃한 분자의 음전하 부분을 끌어당겨 인력이 작용한다.
세기: 쌍극자-쌍극자 힘은 이온 결합(전하의 크기가 더 큼)에 비해 약하다. 이 힘의 세기는 분자의 쌍극자 모멘트가 클수록 증가하며, 이는 끓는점과 같은 물리적 성질을 높인다.
1.2.2. 유발 쌍극자 힘 (Induced Dipole Forces)
정의: 이 힘은 런던 분산력 (London Dispersion Forces)이라고도 하며, 모든 분자(극성 및 비극성) 사이에 존재하는 인력이다.
원리: 분자 내 전자의 순간적인 움직임으로 인해 일시적인 순간 쌍극자(유발 쌍극자)가 발생하고, 이 쌍극자가 이웃한 분자의 전하 분포를 유도하여 일시적인 인력을 발생시킨다.
세기:
분자 크기 및 몰질량: 분자의 몰질량과 크기가 클수록 전자가 핵의 인력으로부터 덜 강하게 붙들려 있어 편극도 (Polarizability)가 증가한다. 따라서 분산력의 세기가 커진다.
분자 모양: 분자 모양이 길고 표면적이 넓을수록 분자간 접촉 면적이 증가하여 분산력이 강해진다.
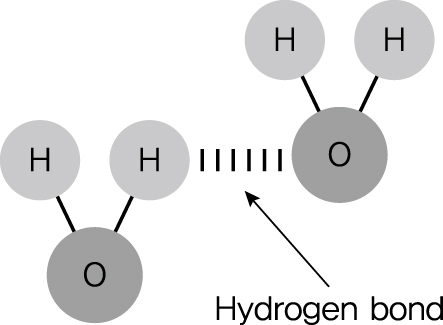
1.2.3. 수소 결합 (Hydrogen Bond)
정의: 쌍극자-쌍극자 상호작용 중 특별히 강한 형태의 인력이다.
조건: 수소 원자가 매우 전기음성도가 큰 원소(
\text{N, O, F} )와 공유 결합을 하고 있을 때, 이 수소 원자가 이웃한 분자의\text{N, O, F} 원자의 고립 전자쌍과 인력으로 결합하는 것이다.
원리:
\text{N-H, O-H, F-H} 결합에서\text{N, O, F} 원자가 전자를 강하게 끌어당기므로,\text{H} 원자는 매우 큰 부분적인 양전하(\delta^+ )를 띠게 되고, 이\text{H} 원자가 이웃 분자의\text{N, O, F} 원자의 부분 음전하(\delta^- ) 및 고립 전자쌍과 강한 인력을 형성한다.
물리적 영향: 수소 결합은 분자간 힘 중 가장 강한 힘에 속하며,
\text{HF}, \text{H}_2\text{O}, \text{NH}_3 와 같은 화합물의 비정상적으로 높은 끓는점과 같은 특이한 물리적 성질을 설명한다.
2. 액체와 고체의 특성 (Characteristics of Liquids and Solids)
2.1. 액체의 성질 (Properties of Liquids)
액체의 독특한 성질은 분자간 힘의 존재와 분자들의 운동성 사이의 균형에 의해 결정된다.
표면 장력 (Surface Tension): 액체의 표면적을 최소화하려는 에너지(
\text{J/m}^2 )를 의미한다.
원리: 액체 내부의 분자는 모든 방향에서 이웃 분자의 인력을 받지만, 액체 표면의 분자는 내부 방향으로만 인력을 받아 표면 분자의 에너지가 높다.
영향: 분자간 힘이 강할수록 표면 장력이 커진다.
점도 (Viscosity): 액체의 흐름에 대한 저항을 의미한다.
원리: 액체 분자들이 강한 인력으로 묶여 있거나, 분자 모양이 복잡하고 엉키기 쉬울 때 분자 이동이 어려워져 점도가 증가한다.
온도 영향: 일반적으로 온도가 높아지면 분자의 운동 에너지가 커져 분자간 힘을 극복하기 쉬워지므로 점도는 감소한다.
모세관 현상 (Capillary Action): 액체가 좁은 관을 따라 상승하거나 하강하는 현상이다.
응집력 (Cohesion): 액체 분자들 사이의 인력이다.
접착력 (Adhesion): 액체 분자와 접촉하는 표면 사이의 인력이다.
원리: 접착력이 응집력보다 강하면 액체가 관을 따라 상승하고, 응집력이 더 강하면 하강한다.
2.2. 고체의 구조 (Structure of Solids)
고체는 분자나 이온이 규칙적인 위치에 고정되어 있는 결정성 고체 (Crystalline Solids)와 불규칙적으로 배열된 비결정성 고체 (Amorphous Solids)로 분류된다.
결정성 고체의 단위 (Unit Cell):
결정 구조는 원자, 이온, 또는 분자가 반복적인 패턴으로 배열된 결정 격자 (Crystal Lattice)로 구성된다.
이 패턴의 가장 기본적인 반복 단위를 단위 세포 (Unit Cell)라고 하며, 결정 구조는 이 단위 세포들이 3차원적으로 쌓여 형성된다.
결정성 고체의 유형:
유형 | 구성 입자 | 결합력 | 특징 | 예시 |
이온성 결정 | 양이온, 음이온 | 이온 결합 (강함) | 녹는점 높음, 단단함, 부서지기 쉬움, 용융 상태에서 전기 전도성 높음 | |
공유 결합 결정 | 원자 | 공유 결합 (매우 강함) | 매우 단단함, 녹는점 높음, 전기 절연체 | 다이아몬드 ( |
분자성 결정 | 분자 | 분자간 힘 (약함) | 녹는점 낮음, 무르고 부서지기 쉬움, 전기 절연체 | |
금속성 결정 | 금속 원자 | 금속 결합 (세기 다양) | 무르거나 단단함, 녹는점 다양, 전기 전도성 및 열 전도성 높음 |
3. 상 변화와 상태도 (Phase Changes and Phase Diagrams)
3.1. 상 변화 (Phase Changes)
정의: 물질이 한 물리적 상태(상)에서 다른 상태로 전환되는 과정이며, 이는 온도 변화나 압력 변화에 의해 발생한다. 상 변화는 흡열 과정(계가 에너지를 흡수)이거나 발열 과정(계가 에너지를 방출)이다.
흡열 과정: 융해(고체
\to 액체), 기화(액체\to 기체), 승화(고체\to 기체).
발열 과정: 응고(액체
\to 고체), 액화(기체\to 액체), 응착(기체\to 고체).
상 변화 엔탈피 (Enthalpies of Phase Changes):
융해열 (
\Delta H_{\text{fus}} ): 고체 1몰이 녹아 액체가 되는 데 필요한 엔탈피 변화이다.
기화열 (
\Delta H_{\text{vap}} ): 액체 1몰이 기화하여 기체가 되는 데 필요한 엔탈피 변화이다.
승화열 (
\Delta H_{\text{sub}} ): 고체 1몰이 승화하여 기체가 되는 데 필요한 엔탈피 변화이며,\Delta H_{\text{sub}} = \Delta H_{\text{fus}} + \Delta H_{\text{vap}} 가 성립한다.
3.2. 액체-기체 평형과 증기압 (Liquid-Gas Equilibrium and Vapor Pressure)
증발 (Evaporation): 액체 표면의 분자가 충분한 운동 에너지를 얻어 액체 상태를 벗어나 기체 상태로 전환되는 과정이다.
증기압 (Vapor Pressure): 밀폐된 용기에서 액체와 기체가 동적 평형 상태일 때, 액체 위의 기체 분자가 나타내는 압력이다.
온도의 영향: 온도가 높아지면 분자의 평균 운동 에너지가 증가하여 더 많은 분자가 증발하므로 증기압은 증가한다.
끓는점 (Boiling Point): 액체의 증기압이 액체에 가해지는 외부 압력과 같아지는 온도이다.
정상 끓는점 (Normal Boiling Point): 증기압이 1 atm일 때의 온도이다.
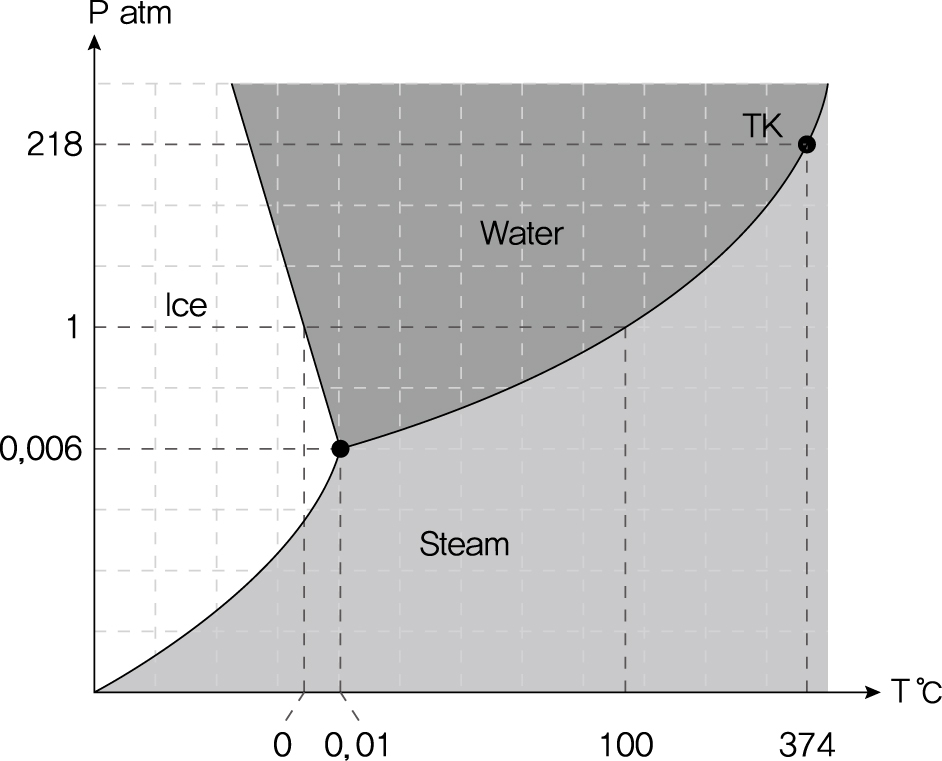
3.3. 상태도 (Phase Diagram)
정의: 물질의 고체, 액체, 기체 상태가 온도와 압력의 함수로써 안정하게 존재하는 조건을 나타낸 도표이다.
주요 특징:
* 상 경계선: 두 상이 평형 상태로 공존하는
* 삼중점 (Triple Point): 세 가지 상(고체, 액체, 기체)이 동시에 평형 상태로 공존하는
* 임계점 (Critical Point): 액체와 기체의 경계가 사라지는
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기