[일반화학]
0
다음 기체 반응은
초기 상태에서
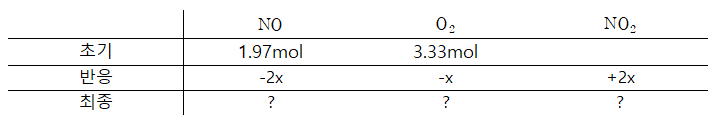
편의를 위해 일단
이를 통해 평형 상수를 계산하면, 다음과 같이 간단해진다.
공학용 계산기의 solve를 사용해 해를 구하게 되면,
※ 실제 이 방정식은 3차방정식으로,
커뮤니티 Q&A
위 문제와 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기[일반화학]
0
다음 기체 반응은
초기 상태에서

편의를 위해 일단
이를 통해 평형 상수를 계산하면, 다음과 같이 간단해진다.
공학용 계산기의 solve를 사용해 해를 구하게 되면,
※ 실제 이 방정식은 3차방정식으로,
커뮤니티 Q&A
위 문제와 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기